新冠中和抗体原理及检测
谈“毒”色变是人类对于病毒一直以来的态度,从埃博拉到SARS,再到如今的2019新型冠状病毒(SARS-CoV-2),无不对人类健康产生了巨大威胁。了解病毒的入侵机制对于研究相应治疗方案必不可少。SARS-CoV-2病毒中有个重要的棘突S蛋白(spike protein),S蛋白是一类由S1/S2异二聚体组成的三聚体跨膜糖蛋白,可识别宿主细胞受体-血管紧张素转换酶2(ACE2)并介导膜融合,其含有的一个C端受体结合域(RBD)更是直接参与了宿主受体的识别,介导病毒入侵宿主细胞。
中和抗体
免疫系统在经受病毒刺激后会产生相应的抗体,有些抗体可以和病毒颗粒结合,阻止病毒感染细胞,以此把病毒“中和”掉了,这些抗体就称为“中和抗体”。也就是说,中和抗体实际上是普通抗体的一种。我们正常所说的抗体是指病毒入侵后机体产生的抗体的统称,它包含针对不同病毒识别表位产生的多个抗体,大部分抗体是通过向T-淋巴细胞发出锁定抗原的信号,激发细胞免疫反应,杀死病毒,而中和抗体则是特异针对病毒中和表位产生的抗体,可直接靶定到病毒中和表位,使病毒失去结合受体的能力,这一过程不需要激活T-淋巴系统。同时研究发现不同结合表位的中和抗体活性也存在差异,其中与病毒中和表位完全吻合的中和抗体活性最好,与病毒中和表位有差异但存在一定覆盖的中和抗体活性显著降低。
在新冠疫情大肆蔓延的背景下,国家科学技术部发布了《新型冠状病毒中和抗体产品研发应急项目申报指南》,申报指南指出中和抗体具备阻断病毒侵染目的细胞的潜力,且单克隆抗体具有作用机制明确、易于大规模产生的优点,是新冠病毒治疗药物研究的重点方向。科学家们纷纷将目光投向了新型疗法---中和抗体疗法。近期由清华大学和深圳国家感染性疾病临床医学研究中心合作,成功从新冠感染者外周血单核细胞中分离出了表达抗体的B细胞,并在人体外实现了抗体表达,获得了2株中和功能较好的单克隆抗体。这种单克隆抗体抗体便是能特异性结合RBD蛋白,并有效阻断病毒与宿主细胞受体ACE2蛋白结合的新冠中和抗体。
2019新型冠状病毒(2019-nCoV)中和抗体的检测方法
新冠中和抗体的检测可以反映群体的感染率、个人的康复情况以及疫苗的效果,但传统的病毒中和实验需使用活病毒和细胞,且对实验室安全性及操作人员技能要求较高。这种耗时长、要求高的传统中和检测方法显示不适用于传播速度快、感染覆盖范围广的新冠疫情。因此,衍生出了几种无需使用感染性病毒、快速检测新冠中和抗体的方法。
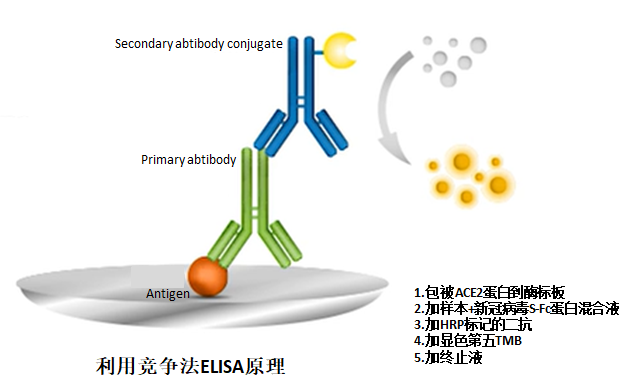
一、酶联免疫吸附法(ELISA)检测
该方法利用新冠病毒蛋白结合结构域RBD抗原和受体蛋白ACE2抗原之间的结合,模拟病毒与宿主细胞的相互作用,通过显色反映判断病毒感染情况,但当中和抗体存在时,便会阻断蛋白互作,显色反应减弱。
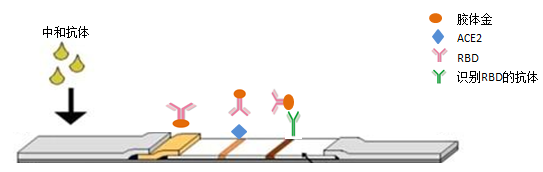
二、胶体金试纸条
胶体金平台利用竞争法检测中和抗体,RBD抗原用胶体金标记并固定在结合垫上,ACE2抗原固定在NC膜的T线上,能与胶体金标记RBD抗原特异结合的抗体固定于NC膜的C线上。当待测样品中有新冠中和抗体时,中和抗体会和RBD抗原结合,降低了RBD和ACE2的结合效率,T线显色度显著下降。
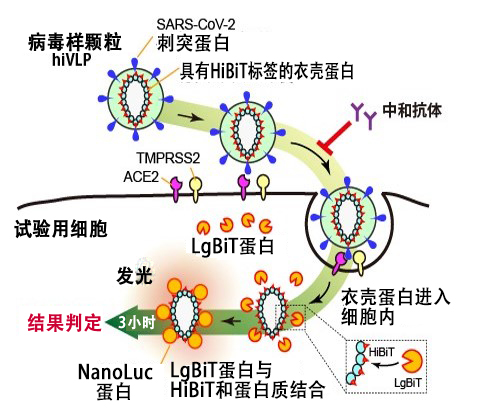
三、hiVNT系统
“hiVNT系统”依赖于一个人为改造的生物发光报告基因NanoLuc荧光素酶,NanoLuc可切分成两个亚基,分别是11aa的小亚基HiBiT和156aa的大亚基LgBiT,两个亚基分开时不具有发光活性,但是融合后又能恢复荧光素酶的活性。 “hiVNT系统”检测新冠中和抗体就是通过组合表达S蛋白和带HiBiT标签的病毒样颗粒VLP,当S蛋白与VeroE6/TMPRSS2细胞表面ACE2受体结合后,VLP膜与宿主细胞膜融合,衣壳蛋白被吸收到细胞中后,HiBiT与宿主细胞中稳定表达的LgBiT蛋白相互作用形成NanoLuc荧光素酶,如果同时添加含中和抗体的血清(如新冠康复期患者的血清),NanoLuc荧光素酶的发光强度显著下降,该检测方法可以作为评价新冠治疗效果的依据。
目前这几种新冠中和抗体检测方法都兼具快速、高通量的特征,可针对性地检测干预治疗后新冠患者体内的中和抗体数量,作为疫苗有效性的检测标准,为后期新冠疫苗大规模筛选提供最合适、最快速的检测方法学。
参考文献
1. Ou X , Liu Y , Lei X , et al. Characterization of spike glycoprotein of SARS-CoV-2 on virus entry and its immune cross-reactivity with SARS-CoV[J]. Nature Communications, 2020, 11(1).
2. Human-IgG-Neutralizing Monoclonal Antibodies Block the SARS-CoV-2 Infection
3. 科技部关于发布新型冠状病毒中和抗体产品研发应急项目申报指南的通知
4. Shi R , Shan C , Duan X , et al. A human neutralizing antibody targets the receptor binding site of SARS-CoV-2[J]. Nature, 2020:1-8.
5. Wang C , Li W , Drabek D , et al. A human monoclonal antibody blocking SARS-CoV-2 infection[J]. Nature Communications, 2020, 11(1).
6. Kei M , Stanleyraj J S , Norihisa O , et al. Rapid quantitative screening assay for SARS-CoV-2 neutralizing antibodies using HiBiT-tagged virus-like particles[J]. Journal of Molecular Cell Biology.



 苏公网安备32011202001302
苏公网安备32011202001302