25-羟基维生素D(25-OH-VD)
该系列产品已获得发明专利,专利号为ZL202311497182.3。

产品参数
| 名称 | 25-羟基维生素D抗体(25-OH-VD antibody) | |
| 货号 | R483k3 | R484j4 |
| 类型 | 单克隆抗体 | |
| 宿主 | 兔 | |
| 反应物种 | 人 | |
| 应用平台 推荐配对 |
化学发光 | 免疫层析 |
| R484j4(捕获)-R483k3(检测) | R483k3(捕获)-R484j4(检测) | |
| 纯度 | Protein A/G纯化,纯度>95% | |
| 缓冲液 | 1xPBS,pH 7.4 | |
| 储存 | -20℃或更低温度,分装保存,避免反复冻融 | |
标记抗体及抗体偶联磁珠
| 名称 | 货号 | 标记/偶联 | 推荐配对 | 推荐平台 |
| 25-羟基维生素D夹心法 (25-OH-VD)标记抗体 |
L216u1 | AE | L217u1(捕获) L216u1(检测) |
化学发光(AE) |
| L217u1 | Biotin | |||
| 25-羟基维生素D夹心法 (25-OH-VD)抗体偶联磁珠 |
B200t1 | 羧基(COOH) 修饰磁珠 |
B200t1(捕获) L216u1(检测) |
|
| B201t1 | 对甲苯磺酰基(Tosyl) 修饰磁珠 |
B201t1(捕获) L216u1(检测) |
||
| B202t1 | 链霉亲和素(SA) 修饰磁珠 |
B202t1(捕获) L216u1(检测) |
发光大包装试剂
| 名称 | 货号 | 推荐平台 | 方法学 |
| 25-羟基维生素D(25-OH-VD)发光大包装试剂 | Q80h1 | 化学发光(AE) | 夹心法 |
解离剂
| 名称 | 货号 | 推荐平台 | 样本稀释比例 |
| 25-羟基维生素D(25-OH-VD)中性解离剂 | D10a1 | 化学发光(AE、ALP) | 10:50 |

产品数据



1.校准曲线——化学发光(AE)平台
用V2.0版、V3.0版25-OH-VD大包装试剂(Q80h1)分别检测浓度范围为0-147.04ng/mL的25-OH-VD校准品,升级后的信噪增益幅度显著提升,尤其是低端。
| 校准品 | 浓度 (ng/mL) |
Q80h1-V2.0版 RLU |
Q80h1-V3.0版 RLU |
| S1 | 0.00 | 254 | 988 |
| S2 | 0.53 | 7866 | 55199 |
| S3 | 2.45 | 48364 | 172199 |
| S4 | 8.97 | 137856 | 363852 |
| S5 | 27.55 | 835688 | 1358846 |
| S6 | 66.23 | 2596874 | 2864657 |
| S7 | 147.04 | 5986321 | 6336428 |
表1.VD校准曲线数据
2.灵敏度——化学发光(AE)平台
用V2.0版、V3.0版Q80h1分别对零浓度稀释液重复测定20次,计算最低检测限,结果显示升级后的Q80h1低端检测灵敏度显著提升。
| 名称 | 浓度 (ng/mL) |
RLU平均值 | 线性方程 |
| 校准品S1 | 0 | 254 | y=14362x+254 |
| 校准品S2 | 0.53 | 7866 | |
| 20次重复测定零浓度稀释液RLU值 | |||
| 658 | 433 | 332 | 448 |
| 455 | 538 | 465 | 432 |
| 369 | 579 | 483 | 695 |
| 488 | 661 | 224 | 455 |
| 493 | 577 | 269 | 387 |
| RLU均值 | 472 | ||
| SD | 124.0 | ||
| 平均值+2SD | 720 | ||
| 最低检测限(ng/mL) | 0.032 | ||
表2.最低检测限(Q80h1-V2.0版)
| 名称 | 浓度 (ng/mL) |
RLU平均值 | 线性方程 |
| 校准品S1 | 0 | 988 | y=102285x+988 |
| 校准品S2 | 0.53 | 55199 | |
| 20次重复测定零浓度稀释液RLU值 | |||
| 1033 | 946 | 1103 | 894 |
| 1055 | 973 | 964 | 1022 |
| 1084 | 966 | 933 | 1036 |
| 1058 | 1024 | 964 | 1055 |
| 998 | 1138 | 1105 | 1094 |
| RLU均值 | 1022 | ||
| SD | 66.0 | ||
| 平均值+2SD | 1154 | ||
| 最低检测限(ng/mL) | 0.002 | ||
表3.最低检测限(Q80h1-V3.0版)
3.相关性——化学发光(AE)平台
用V2.0版、V3.0版Q80h1分别检测82例质谱赋值样本(浓度范围7.69~57ng/mL),样本符合率(R2)分别为0.951和0.9803,升级后样本符合率显著提升。
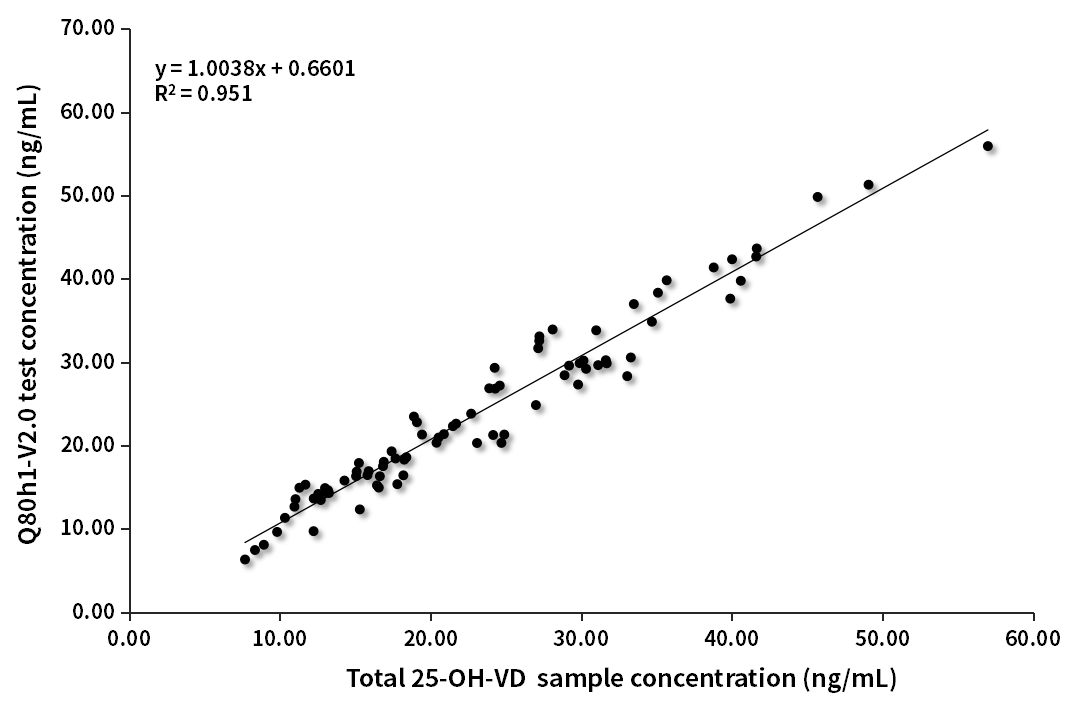
图1.VD临床对比分析(质谱赋值-V2.0版)
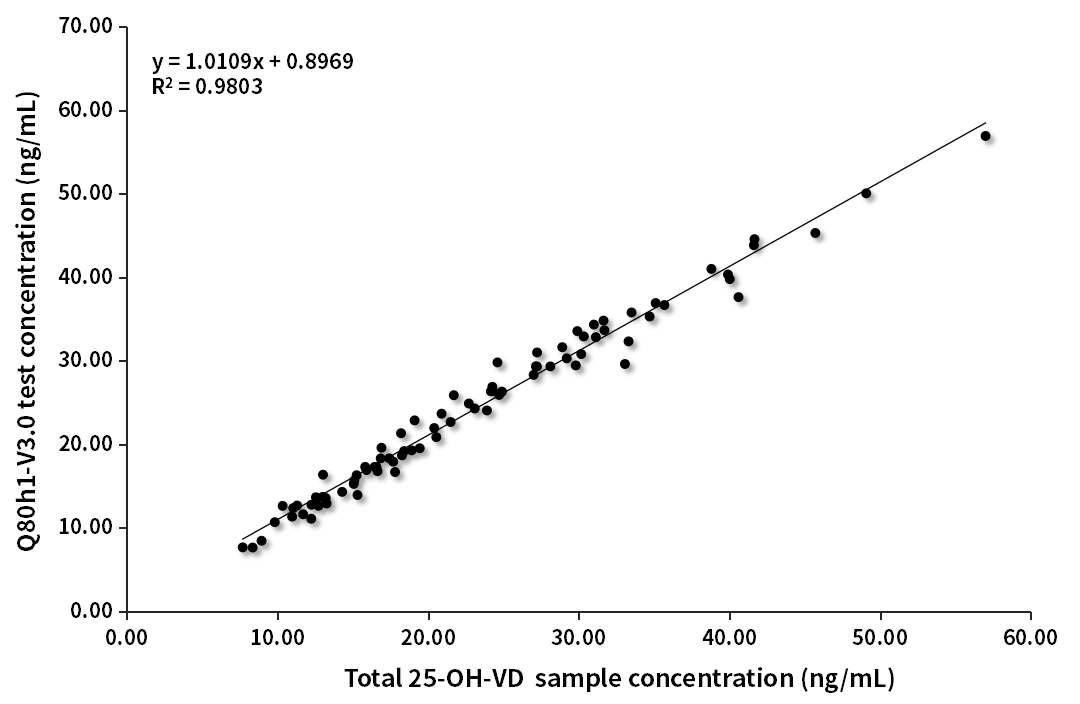
图2.VD临床对比分析(质谱赋值-V3.0版)
| 编号 | 样本浓度 (ng/mL) |
检测浓度 (ng/mL) |
| 1 | 7.69 | 6.34 |
| 2 | 8.35 | 7.48 |
| 3 | 8.94 | 8.11 |
| ︙ | ︙ | ︙ |
| 81 | 49.08 | 51.31 |
| 82 | 57 | 55.94 |
表4.VD临床对比分析数据(质谱赋值-V2.0版)
| 编号 | 样本浓度 (ng/mL) |
检测浓度 (ng/mL) |
| 1 | 7.69 | 7.68 |
| 2 | 8.35 | 7.66 |
| 3 | 8.94 | 8.47 |
| ︙ | ︙ | ︙ |
| 81 | 49.08 | 50.08 |
| 82 | 57 | 56.95 |
表5.VD临床对比分析数据(质谱赋值-V3.0版)
4.试剂37℃7天热加速稳定性——化学发光(AE)平台
将V2.0版、V3.0版Q80h1放置在37℃条件下,分别在0、7天时,去检测低值和高值质控品。V2.0版试剂测得的低值质控品浓度7天跌幅为8%,高值质控品跌幅9.92%。V3.0版试剂测得的低值质控品7天跌幅为3%,高值质控品跌幅2.18%。升级后的Q80h1热加速稳定性大幅提升。
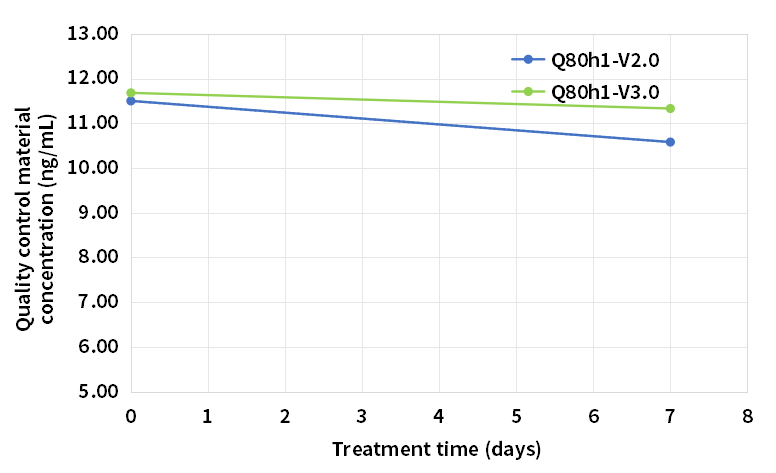
图3.试剂37℃7天热加速稳定性(低值质控)
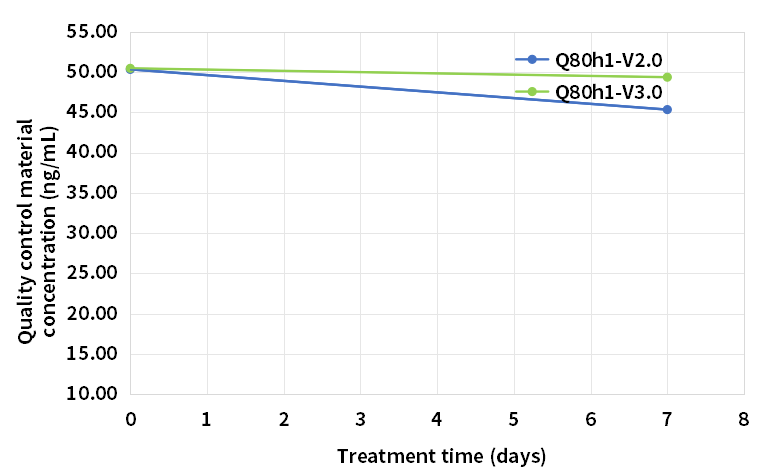
图4.试剂37℃7天热加速稳定性(高值质控)
5.校准品稳定性——化学发光(AE)平台
由于小分子不稳定,市面上主流的VD检测试剂配套校准品多采用冻干技术储存,通常冻干后复溶稳定性无法保障,且成本高。欧凯V3.0版25-OH-VD大包装试剂配备的是液体校准品,无需冻干,且开瓶稳定(见图5、6),机载友好;2-8℃至少可以保存1年。此外,校准品37℃7天热加速稳定性也依然优秀,低值跌幅为3.2%,高值跌幅为2.4%(未展示)。
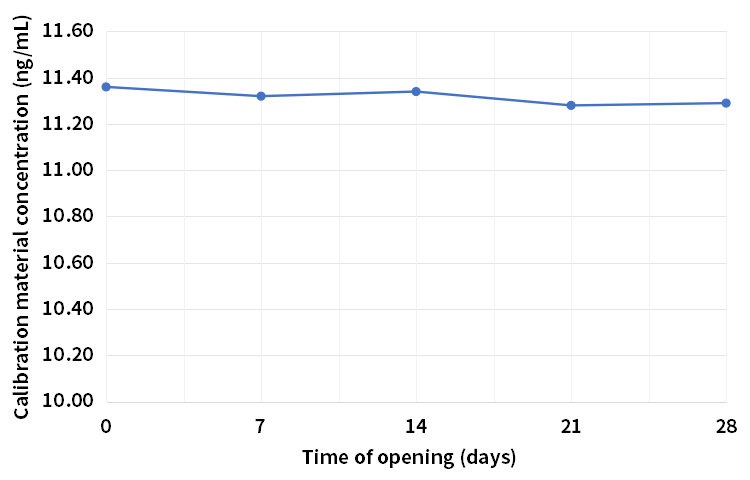
图5.低值校准品28天开瓶稳定性
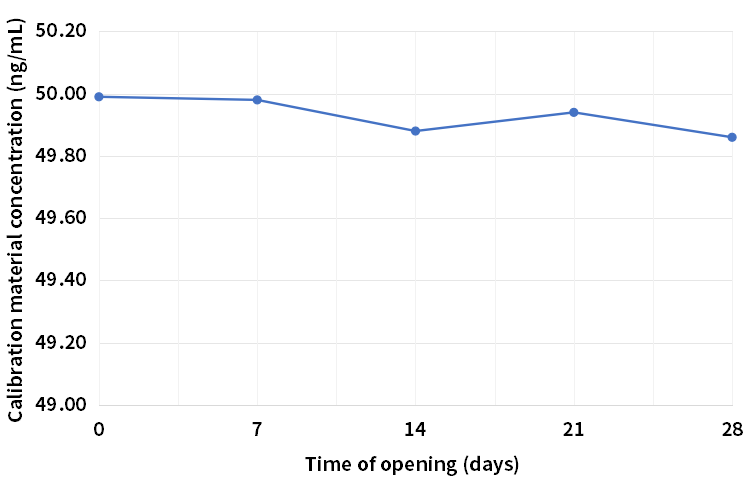
图6.高值校准品28天开瓶稳定性

为满足客户需求,打造高品质试剂,结合市场调研和用户反馈意见,南京欧凯生物对25-OH-VD发光大包装试剂(Q80h1)的核心原料及试剂性能进行了全方位的优化。升级版Q80h1试剂检测灵敏度与线性兼具;在降低非特异性背景噪音的同时,大幅提高信号强度。与初代试剂相比,整体信噪比提升约45倍。


1.超强信噪比
Q80h1采用新一代小分子夹心检测技术,其检测灵敏度和特异性都显著优于竞争法,但在线性和背景噪音方面却仍有优化空间。为此,我们对Q80h1的核心原料进行了升级,升级后的背景噪音有效降低,信号增益幅度更大,区分度也更高。低端信噪比提升了15倍,高端信噪比提升了近45倍。
| 校准品 | 浓度 (ng/mL) |
RLU |
| S1 | 0.00 | 195 |
| S2 | 1.15 | 12217 |
| S3 | 3.44 | 26591 |
| S4 | 15.71 | 208683 |
| S5 | 31.91 | 842490 |
| S6 | 70.33 | 2731118 |
| S7 | 153.86 | 6567286 |
| S2/S1 | 62.65 | |
| S6/S1 | 14005.73 | |
表1.25-OH-VD信噪比(升级后)
| 校准品 | 浓度 (ng/mL) |
RLU |
| S1 | 0.00 | 14776 |
| S2 | 0.22 | 19850 |
| S3 | 1.08 | 55912 |
| S4 | 10.27 | 534999 |
| S5 | 45.02 | 2464797 |
| S6 | 75.15 | 4585520 |
| S3/S1 | 3.78 | |
| S6/S1 | 310.34 | |
表2.25-OH-VD信噪比(升级前)
2. 比标质谱金标准
用Q80h1检测106例质谱赋值样本(浓度范围7.69~57ng/mL),样本符合率(R2)可达0.9645。
| 编号 | 质谱检测浓度 (ng/mL)) |
自测浓度 (ng/mL) |
| 1 | 7.69 | 6.89 |
| 2 | 8.35 | 9.8 |
| 3 | 8.94 | 10.21 |
| ︙ | ︙ | ︙ |
| 105 | 49.08 | 54.77 |
| 106 | 57 | 54.38 |
表3.VD临床对比分析数据(质谱赋值)
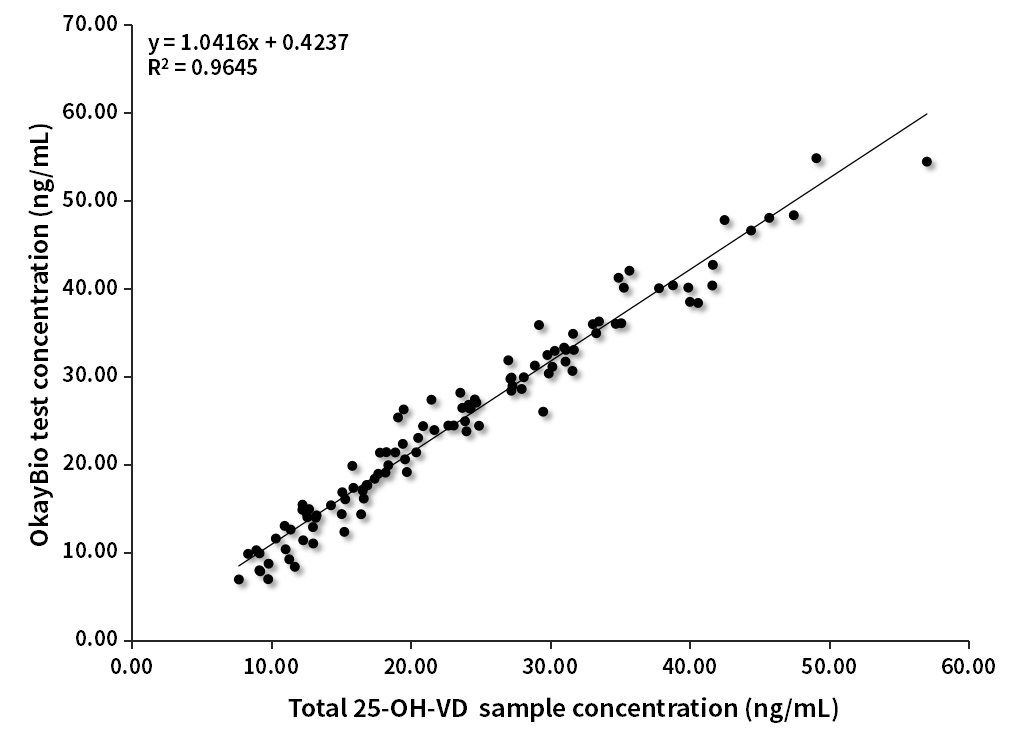
图1.VD临床对比分析(质谱赋值)
3. 检测VD2高浓度样本同样精准
临床研究显示:市售五大主流品牌(雅培、DiaSorin、IDS、罗氏、西门子)的25-OH-VD检测试剂与LC-MS/MS检测结果临床判定一致率不到71%。当样本中含有25-OH-VD2时,与LC-MS/MS检测结果的相关性更低。
为验证Q80h1对含有高浓度25-OH-VD2样本的检测能力,我们选取了11例25-OH-VD2含量明显高于25-OH-VD3的VD质谱赋值样本。用Q80h1和一款市售主流竞争法VD试剂同时对这些样本进行检测。结果显示:Q80h1的检测结果与质谱符合率依然很高(R2=0.939),而竞争法检测结果与Q80h1、质谱均存在明显偏差。
表4.VD临床对比分析数据(质谱赋值VD2高浓度样本)
化学发光平台(AE)
1.总25-OH-VD识别能力
25-OH-VD抗体对25-OH-VD2的识别能力直接影响总25-OH-VD检测结果的准确性。经验证欧凯25-OH-VD发光大包装试剂(Q80h1)与25-OH-VD2、25-OH-VD3有很好的反应性,可有效识别样本中的总25-OH-VD。
| 浓度 (ng/mL) |
RLU | |
| 25-OH-VD2 | 25-OH-VD3 | |
| 0.00 | 201 | 213 |
| 5.03 | 33900 | 21043 |
| 15.16 | 228481 | 155393 |
| 35.43 | 951458 | 780271 |
| 70.12 | 2720547 | 2188499 |
| 150.73 | 6429867 | 5647803 |
表5.总25-OH-VD识别能力数据
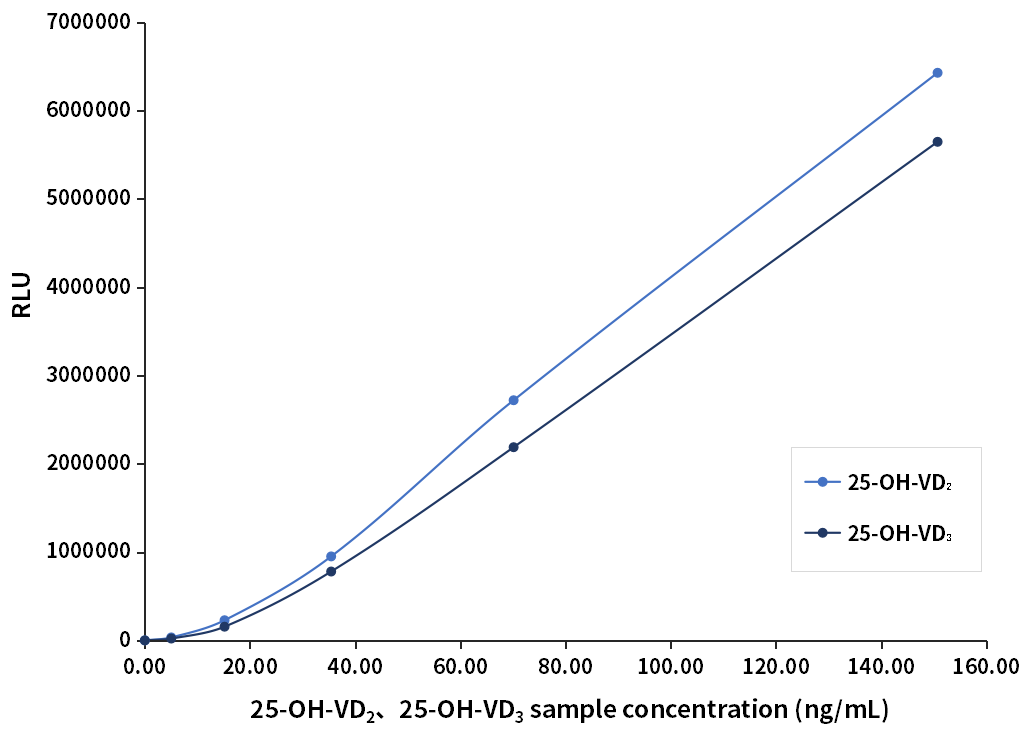
图2.总25-OH-VD识别能力
2.最低检测限
用Q80h1对零浓度稀释液重复测定20次,计算最低检测限。
| 名称 | 浓度(ng/mL) | RLU平均值 | 线性方程 |
| 校准品S1 | 0.00 | 195 | y=10454x+195 |
| 校准品S2 | 1.15 | 12217 | |
| 零浓度稀释液20次重复测定RLU值 | |||
| 213 | 231 | 198 | 245 |
| 205 | 241 | 193 | 265 |
| 230 | 205 | 249 | 232 |
| 232 | 232 | 208 | 322 |
| 225 | 216 | 230 | 316 |
| RLU均值 | 234 | ||
| SD | 34.1 | ||
| 平均值+2SD | 303 | ||
| 最低检测限(ng/mL) | 0.010 | ||
表6.VD发光大包装试剂最低检测限
3.线性
将浓度为148ng/mL的质谱赋值高浓度样本用样本稀释液稀释为50%、20%、10%、5%和1%五个浓度。用Q80h1对高浓度样本及五个稀释样本进行检测,计算相关性。
| 百分比 | 浓度(ng/mL) | RLU | 绝对偏差 | 相对偏差 |
| 100% | 148 | 6399087 | / | 0.60% |
| 50% | 71.3 | 2961553 | / | -3.10% |
| 20% | 30.9 | 754539 | / | 4.70% |
| 10% | 14.2 | 190843 | -0.62 | / |
| 5% | 8.30 | 60302 | 0.83 | / |
| 1% | 1.41 | 15120 | -0.18 | / |
| 相关性:0.99971 | ||||
表7.VD发光大包装试剂线性
4.重复性
利用同一批Q80h1对浓度为10.26ng/mL和50.31ng/mL的质谱赋值样本各重复检测10次,其测量浓度变异系数(CV)均小于3%。
| 低值样本 | ||
| 测定值编号 | RLU | 浓度(ng/mL) |
| 1 | 97500 | 10.32 |
| 2 | 96880 | 10.28 |
| 3 | 94734 | 10.14 |
| 4 | 97811 | 10.34 |
| 5 | 93522 | 10.06 |
| 6 | 94886 | 10.15 |
| 7 | 104663 | 10.77 |
| 8 | 97966 | 10.35 |
| 9 | 95344 | 10.18 |
| 10 | 107463 | 10.94 |
| 平均值 | / | 10.35 |
| 标准差 | / | 0.28 |
| CV | 2.7% | |
表8.VD发光大包装试剂重复性(低值)
| 高值样本 | ||
| 测定值编号 | RLU | 浓度(ng/mL) |
| 1 | 1731067 | 50.24 |
| 2 | 1810231 | 51.83 |
| 3 | 1752956 | 50.68 |
| 4 | 1713169 | 49.88 |
| 5 | 1785816 | 51.34 |
| 6 | 1738030 | 50.38 |
| 7 | 1741512 | 50.45 |
| 8 | 1762412 | 50.87 |
| 9 | 1726412 | 50.14 |
| 10 | 1726094 | 50.31 |
| 平均值 | / | 50.61 |
| 标准差 | / | 0.592 |
| CV | 1.17% | |
表9.VD发光大包装试剂重复性(高值)
5.准确度
将浓度为50.31ng/mL的质谱赋值高浓度样本,按照1:9的体积比加入到浓度为10.15ng/mL的低浓度血清中,配制成浓度为14.17ng/mL的混合物,用Q80h1进行检测,计算回收率。
| 待测物 | 测定浓度(ng/mL) | RLU | 浓度平均值 (ng/mL) |
| 高浓度样本 | 50.35 | 1736538 | 50.42 |
| 50.22 | 1730072 | ||
| 50.68 | 1752956 | ||
| 低浓度血清 | 10.12 | 94430 | 10.22 |
| 10.21 | 95803 | ||
| 10.34 | 97811 | ||
| 混合物 | 14.16 | 170846 | 14.26 |
| 14.32 | 174539 | ||
| 14.29 | 173842 | ||
| 回收率 | 100.28% | ||
表10.VD发光大包装试剂回收率
6.热稳定性
将Q80h1试剂组份分别放置于37℃培养箱和4℃冰箱中加速7天,分别测试高、低值样本,比较其偏差。
| 低值样本 | ||||
| 测定值 编号 |
RLU | 浓度(ng/mL) | ||
| 4℃7天 | 37℃7天 | 4℃7天 | 37℃7天 | |
| 1 | 93071 | 84504 | 10.03 | 9.44 |
| 2 | 94886 | 85490 | 10.15 | 9.51 |
| 3 | 92921 | 85207 | 10.02 | 9.49 |
| 偏差 | / | -5.8% | ||
表11.VD发光大包装试剂热稳定性(低值)
| 高值样本 | ||||
| 测定值 编号 |
RLU | 浓度(ng/mL) | ||
| 4℃7天 | 37℃7天 | 4℃7天 | 37℃7天 | |
| 1 | 1736040 | 1635741 | 50.34 | 48.32 |
| 2 | 1725100 | 1637724 | 50.12 | 48.36 |
| 3 | 1738527 | 1632272 | 50.39 | 48.25 |
| 偏差 | / | -4.1% | ||
表12.VD发光大包装试剂热稳定性(高值)

试用申请

VD临床诊断意义
维生素D(Vitamin D,VD)是人体健康、生长和发育必不可少的物质,其缺乏或过量与多种疾病密切相关,如骨骼肌肉疾病、呼吸系统疾病、心血管疾病、免疫性疾病、肾脏疾病、神经精神疾病等。
维生素D是一种类固醇激素, 通过调节肠道吸收和肾脏重吸收作用维持机体的钙平衡。维生素D主要包括2种类型:维生素D2(VD2)和维生素D3(VD3),VD2主要通过摄取食物获得(约占VD总量的10%),VD3主要通过日光中的紫外线照射皮肤产生。体内维生素D通过与白蛋白和VD结合蛋白结合后经血液运送至肝脏, 在肝脏分泌的25-羟化酶的参与下, 25号位羟化过程并形成25-(OH)-VD。在肾脏中, 25-(OH)-VD进一步被1α -羟化酶转化成具有生物活性的1, 25(OH)2VD3(1, 25-dihydroxyvitamin D3, 又称骨化三醇)。最后在DBP转运蛋白的载运下,经血液到达小肠、骨等靶器官中与靶器官的核受体(VDRn)或膜受体(VDRm)结合,发挥相应的生物学效应。
25-(OH)-VD是机体维生素D的主要储存形式, 占VD总量的95%以上。由于其半衰期长(2 ~ 3周), 并且不受血钙和甲状旁腺素水平的影响, 因此被公认为是客观评价体内VD含量的最佳指标。
| 体内25羟基维生素D含量(ng/ml) | 临床建议 |
|---|---|
| <10 | 严重缺乏 |
| 10-20 | 缺乏 |
| 20-30 | 不足 |
| 30-100 | 正常 |
参考文献
1.B. Oliveri, A.G. Díaz, M. González Pernas,等. Serum 25OHD levels in adults living in the city of Buenos Aires: Importance of vitamin D supplementation[J]. Bone, 2016, 89:64.
2.Adriana S. Dusso, Alex J. Brown, Eduardo Slatopolsky. Vitamin D[J]. 2005, 289(1):F8-28.
3.Lips, Paul, Graafmans, Wilco C. Vitamin D supplementation and fracture incidence in elderly persons[J]. Annals of Internal Medicine, 1996, 124(4):400-406.
4.向伟, 丁宗一, 郑维. 维生素D及其受体与临床相关疾病的研究[J]. 中华儿科杂志, 2004(7).

相关产品



 苏公网安备32011202001302
苏公网安备32011202001302