美国甲状腺协会对甲状腺刺激激素、甲状腺激素临床和实验室现状的回顾(2023)
——TSH及T3、T4检测的分析性能
背景
尽管甲状腺检测是实验室内分泌研究最多的,但甲状腺检测(促甲状腺素[TSH]和甲状腺激素[TH]测量)的最佳使用仍有争议,这些检测结果的解释可能含糊不清。美国甲状腺协会(ATA)从专业知识方面给予美国疾病控制中心(CDC)和国际临床化学和检验医学联合会(IFCC)支持,以改善和维持甲状腺检测的标准化和统一。ATA授权了一个国际跨学科工作小组,通过最近的文献来调查甲状腺检测的现状,以便根据需要修改或更新标准,并为临床护理提供信息。
1. 甲状腺检测的分析性能规范(APS)
甲状腺功能检测,像大多数实验室检测一样,容易出现测量结果不准确的情况。实验室测量可能受到两种不同类型的分析误差影响:(1)系统误差(也称为分析偏差)和(2)随机误差(也称为分析不精确)。所谓测量总误差就是这两个参数的综合。分析错误可能导致错误的实验室结果,进而导致不适当的疾病分类和临床决策。为了防止不准确的测量影响临床决策,已经建立了分析性能规范(APS)来保障分析性能。
APS可用于优化实验室检测多方面的临床效用,包括实验室检测批准的监管流程、单个实验室的熟练程度、实验室方法的评估以及监测批次间试剂变化的可变性。APS可以基于(1)临床结局研究和对临床决策的影响(分别为模型1a和1b);(2)生物变异(模型2);(3)最先进的实验室性能(模型3)。目前只有有限的研究检验了APS对临床结果或医疗决策的影响,所以模型2、3是定义APS的主要依据。另外,最先进的APS可以从实验室方法的评估和比较,或者同行能力测试项目的比较数据中获得。
总的来说,目前TSH检测在临床实践中的应用符合理想APS(基于生物变异)的不精确性,但fT4则并非如此。TSH和fT4检测都观察到较大的方法间偏差。这将不利于甲状腺检查的通用参考区间设置,同时也限制了医疗决策。此外,TSH和fT4之间的关系取决于所使用的具体检测方法。
2. 甲状腺检测的生物学变异性
TSH-fT4的对数线性关系说明了健康个体体内和受试者之间的生物学变异性;这种变异性在甲状腺和非甲状腺疾病中都有所增加,对健康的单卵和异卵双胞胎进行系统研究的结果,重复抽样研究以及对不同地区的个体或(亚)人群的测试表明,受试者内部的变异性(例如每月抽样期间的变异性)明显小于受试者之间的变异性。这些研究表明,TSH、fT4、fT3和fT4×TSH产品的遗传性占变异性的30% - 65%。基于人群的甲状腺测试变量的参考区间要比受试者内差异宽得多。
表1. 基于生物变异的分析性能指标的数学定义
| 分析性能规范 | 说服力 | 公式 |
| 不精确(CVa,%) | 最低 | 0.75 x CVi(%) |
| 合适 | 0.50 x CVi(%) | |
| 最佳 | 0.25 x CVi(%) | |
| 偏差(%) | 最低 | 0.375 x(CVi2 + CVg2)0.5 |
| 合适 | 0.250 x(CVi2 + CVg2)0.5 | |
| 最佳 | 0.125 x(CVi2 + CVg2)0.5 | |
| 总误差 | 偏差 + 1.65 x 不精确度 |
注:其中CVa为分析变异,CVi为受试者内生物变异,CVg为受试者间生物变异。
表2. 基于生物变异数据的分析性能规范
| 激素 | CVi(%) | CVg(%) | 参数 | 最低 | 合适 | 最佳 |
| TSH | 18(15-29) | 36(24-48) | 偏差(%) | 15 | 10 | 5 |
| 不精确度(%) | 13 | 9 | 4 | |||
| 总误差(%) | 37 | 25 | 12 | |||
| fT4 | 4.8(4.8-9.5) | 7.7(7.5-12.1) | 偏差(%) | 3.5 | 2.3 | 1.2 |
| 不精确度(%) | 3.7 | 2.5 | 1.2 | |||
| 总误差(%) | 9.5 | 6.3 | 3.2 |
注:基于生物变异数据荟萃分析(括号中为估计的95%置信区间)的分析性能规范,由欧洲临床化学和实验室医学生物变异工作组联合策划。
3. 甲状腺检测的可比性和质量评价
鉴于对患者疾病的诊断、治疗和监测具有很高的临床影响,激素测定的结果必须可靠。因此,保证它们的特异性、准确性和精密度需要外部参考、标准和认证的参考物质,以及定期记录的熟练程度测试。每个实验室使用的方法应符合国际指南ISO 17511:2020,以保证患者样本的结果可追溯到SI单位或最高可用标准。
3.1 检测结果的可比性
理想情况下,TH实验室结果应在不同时间、地点均具有可比性,且与所使用的方法无关。2017年,国际临床化学和检验医学联合会甲状腺功能测试标准化委员会(IFCC C-STFT)记录了13家检测制造商fT4和TSH检测结果的可比性状况。由于分析试剂和设备差异,fT4和TSH的实验室结果可能相差高达50%(图1)。如果不采用特定方法的参考区间,测试结果的数值分类也可能会因使用的分析方法而不同。
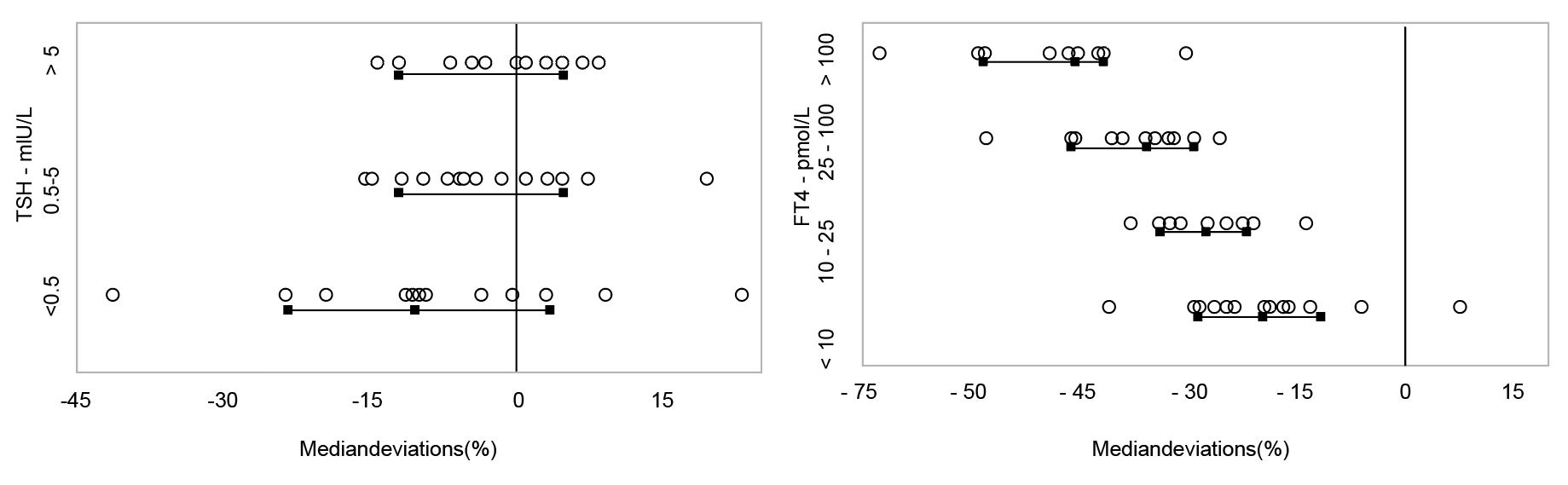
图1. 2017年国际临床化学和检验医学联合会甲状腺功能测试标准化委员会记录的
TSH和fT4检测结果的可比性
注:显示了约100个患者血清样本浓度分布在整个测量间隔内与参考值每次测定的中位数偏差(黑线和方框表示:15、 50、85百分位;垂直线表示:参考游离甲状腺素:基于平衡透析-同位素稀释-质谱法的候选参考测量程序/参考促甲状腺素:所有程序平均值)。修改和更新自Thienpont等和De Grande等,请参阅原始出版物了解详情。
C-STFT提出了一种改善现状的方法,根据ISO 17511建立的参考测量系统标准化fT4和统一TSH检测。研究表明,对于fT4和TSH检测标准化/统一的实施可以减少制造商之间的校准差异。fT4值标准化对患者结果和参考区间的预期影响可达30-50%,因此标准化前需要精心筹划。
3.2 分析方法的质量评价
3.2.1 材料的可交换性
有效质量评估的先决条件是所用材料的可交换性,用于质量评估的材料应该在任何给定的分析中表现得与任何患者样本完全相同。市售的熟练度测试材料和质控品很少复制临床相关的基质及其可变性。这已经在一项TSH参考物质的研究中得到证实,无论是从人垂体组织中提取的TSH,还是重组表达(糖工程)的TSH都不能精确匹配甲状腺功能减退患者的唾液化TSH。同样,fT4参考物质基质也不同于非甲状腺疾病、脂质代谢紊乱或肾脏疾病患者的血清或血浆,这种基质差异将限制检测结果的可比性,这种限制也许可以通过标准化程序解决。
3.2.2 SI单位
在临床实践中一直使用非SI单位(例如ng/dL),而不是正确的SI单位(mol/L),经常造成混淆。特别是将T4的浓度范围与T3的浓度范围进行比较时。TH在血液的血清中循环,因此测量结果应表示为单位体积血清中存在的摩尔量。
C-STFT的研究始于2017年,关于当前fT4和TSH检测准确性和质量的信息非常有限。一些信息可以从基于准确性的外部质量评估/能力测试程序中获得。其他信息可以从门诊数据(例如,Noklus百分位)或匿名电子病历中获得。监测甲状腺功能检测的准确性,需要使用不同来源的数据进行更多的研究。
4.甲状腺检测的分析有效性
免疫测定或常规LC-MS方法性能的最佳验证是通过与参考测量程序进行比较,如FT4和TSH测定的可比性和质量评估部分所述。在此之前,应评估分析设计、线性、检出限、精密度、交叉反应性等方面的基本分析有效性。临床和实验室标准协会(CLSI)已经发布了多个国际公认的指南和协议,与甲状腺检测相关的是游离激素测定的CLSI C45-A和液相色谱-质谱法的CLSI C62Ed2标准。
样品中未知的交叉反应化合物可能无法通过免疫分析识别并返回假值,而充分建立的LC-MS方法不会被交叉反应物影响。竞争性免疫分析的先决条件是标记的分析物类似物,其具有与分析物相似的免疫学特性。分析物的化学修饰如生色基团标记和碘化,通常用于生产分析示踪剂。这些修饰可能影响示踪剂的免疫反应性和交叉反应性。对于T4和T3,碘甲状腺原氨酸的4'-OH基团或丙氨酸侧链功能的任何修饰(通常用于非放射性TH IA)都可能影响Ab的识别和反应性,但自然产生的127-I取代基被放射性同位素125-I取代,则没有影响。
参考文献
Van Uytfanghe K, Ehrenkranz J, Halsall D, et al. Thyroid Stimulating Hormone and Thyroid Hormones (Triiodothyronine and Thyroxine): An American Thyroid Association-Commissioned Review of Current Clinical and Laboratory Status[J]. Thyroid. 2023, 33(9): 1013-1028.

相关产品



 苏公网安备32011202001302
苏公网安备32011202001302