基于NGS的分子诊断
分子诊断是应用分子生物学方法,通过检测受检个体或其携带病毒、病原体的遗传物质的结构或含量变化而做出诊断的技术,而基于下一代测序(Next Generation Sequencing,NGS)的分子诊断被广泛应用于传染性疾病、血液筛查、遗传性疾病、肿瘤伴随诊断等领域。相比于免疫诊断技术,NGS在发现未知基因、液体活检方面具有优势,但目前存在明显局限性,如对基础设施要求高、结果的准确性和可重复性存在问题等。
1. NGS概述
自Sanger测序后,NGS技术显著发展,可提供更高的数据输出、效率和应用。将DNA(或cDNA)随机片段化、加接头,制备测序文库,通过对文库中数以万计的克隆进行延伸反应,检测对应的信号,最终获取序列信息。NGS在处理大规模样品时具有显著的优势,成为目前组学研究的主要技术。
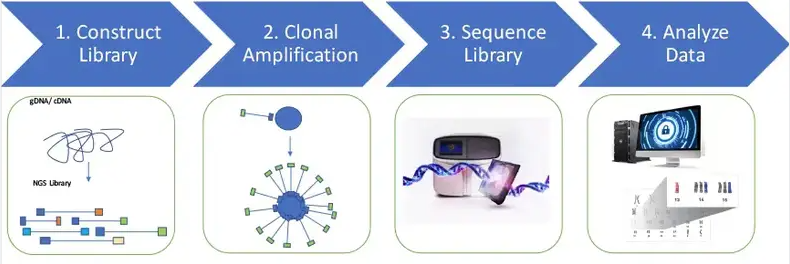
Fig.1 NGS基本流程
1.1 文库制备
NGS的先决条件是高质量的文库。文库制备首先需获得与测序所需分子相对应的模板,然后制备片段使其与所使用的测序平台兼容。测序可分为DNA测序(DNA-Seq)和RNA测序(RNA-Seq)。文库大小是由插入片段(接头序列之间的文库部分)大小决定的,最佳插入片段长度是由NGS设备以及特定测序应用决定的。
1.1.1 DNA文库制备
根据测序模板,DNA-Seq可以包括全基因组测序(WGS)、全外显子组测序(WES)、表观基因组测序或靶向测序(TS)。模板制备包括聚合酶链式反应(PCR)和基于杂交捕获的方法。
- PCR常用于制备TS模板。在早期阶段,扩增子测序侧重于有限数量的基因或外显子(短程PCR)。长程PCR(LR-PCR)的出现使鸟枪测序(对随机断裂的、比扩增子短的片段进行测序)成为一种主要方法。因此,LR-PCR改善了短扩增子测序中出现的序列模糊问题。
- 杂交捕获常用于制备WES和TS模板,其中互补的生物素化探针与目标区域杂交,使用链霉亲和素包被的磁珠进行分离。与PCR相比,这种富集方法对于较大基因组区域是一种经济高效的方法,同时减少了等位基因丢失。
DNA-Seq文库构建涉及片段化、末端修复、接头连接和大小选择的核心步骤。DNA片段化将DNA剪切成最佳的特定尺寸范围,三种断裂方法包括物理(即超声处理)、酶促(即断裂酶或转座酶破碎)或化学(二价金属阳离子加热)方法。较小的片段有助于高质量的测序数据,而较长的片段则提供远端相位信息。
起始DNA被片段化后,会使用T4多聚核苷酸激酶、T4 DNA聚合酶以及Klenow片段三种酶的混合物进行末端补平和5'端磷酸化。3'端利用Taq DNA聚合酶或Klenow片段加A尾。片段化后产生5'/3'黏性末端及平末端,粘性末端都需转化为平末端。在使用TA连接的方式进行接头连接时,DNA片段在5'端磷酸化后使用Taq DNA聚合酶在3'端加“A”与带“T”黏性末端的接头互补配对。接头连接后,PCR富集通常与文库制备步骤相结合。PCR通常使用高保真聚合酶,该酶具有5'→3'聚合酶活性,可沿5'→3'方向合成DNA,同时具有的3'→5'核酸外切酶活性,可去除新合成的DNA链或引物3'端的不匹配碱基。
1.1.2 RNA-seq文库制备
对于RNA文库,需要根据测序目的进行文库构建方案的筛选。如果目的是发现复杂全面的转录,文库需要覆盖整个转录组,包括编码、非编码、反义及基因间RNA。RNA-Seq对于功能基因组研究非常有用,例如差异基因表达、选择性剪接和变异发现。RNA-Seq可分为全转录组测序(WTS)、mRNA测序(mRNA-Seq)和小RNA测序(smRNA-Seq)。样品制备一般包括三个步骤:总RNA分离、靶RNA富集以及RNA反转录成互补DNA(cDNA)。
cDNA合成
RNA需经过反转录形成cDNA的第一条链,因RNA极易被环境中存在的RNase降解,在反转录过程中使用RNase Inhibitor可以抑制这些酶的活性,保护RNA不被RNase降解。与此同时,逆转录酶将模板RNA反转录成cDNA;逆转录酶具有依赖RNA的DNA聚合酶活性,能够以RNA为模板,按5'→3'方向合成一条与RNA模板互补的DNA单链,也就是cDNA第一链。
cDNA第二链合成时,RNase除去RNA-DNA杂交链中的RNA链,配合DNA聚合酶催化合成。DNA聚合酶具有5'→3'DNA聚合酶活性,可在模板和引物的作用下,沿5'→3'方向合成与cDNA一链互补的序列。随后进行末端修复、接头连接、PCR扩增最终产生cDNA文库。
2. NGS的临床应用
随着精准医疗概念的提出,临床应用上对NGS的需求越来越大,病原学诊断、检测与遗传病、肿瘤等疾病的精准诊断等应用领域对NGS的要求也越来越高。在发生的几次世界性范围的传染性疫情中,NGS技术也逐渐扮演起重要的角色。
2.1 临床微生物病原学诊断
人体中有着由细菌、真菌、病毒等微生物组成的庞大而复杂的胃肠道系统,且人体许多疾病的发生都与微生物系统的失调或微生物入侵有着极其紧密的关系,而NGS技术的出现为这些微生物菌群的鉴定检测与研究提供了有力的技术支持。
2.2 临床微生物耐药诊断
临床上,医院获得性感染的细菌用药治疗一直是医疗难点,主要是由于在长期的抗生物用药筛选中,许多病原体通过基因突变获得对不同抗生素的耐药性,给临床治疗造成了极大影响。目前,通过高通量测序深度挖掘并组建药学相关微生物组学数据库,根据数据库发现超过60种药物与微生物之间存在相互作用。后期高通量测序也可持续挖掘微生物耐药性、微生物与药物间相互作用及其与人类遗传变异的相关性。
2.3 临床肿瘤诊治
在癌症预防上,高通量测序平台可以用于肿瘤基因的突变筛查,指导癌症的防控工作;在癌症治疗上,通过高通量测序平台挖掘与癌症相关的基因,不仅可以发掘与癌症相关的诊断靶标,还可以发掘与之相关的治疗靶点,为临床提供具体的个性化用药指导。
2.4 遗传疾病诊断检测
NGS的另一项较为重要的应用是遗传性疾病的检测诊断,主要包括遗传病诊断、产前筛查与诊断及植入性胚胎遗传学诊断。对产妇进行无创产前基因检测(NIPT),然后对基因检测异常的产妇羊水或脐带血细胞进行染色体G显带检测和荧光原位杂交检测,作为确诊标准。NGS为遗传性疾病诊断、新生儿疾病早期诊断、产妇无创检测都提供了极大的便利,在遗传性疾病的治疗与预防方面呈现出很大的临床应用价值。
表1. NGS平台的临床应用
| 应用领域 | 应用方向 | 应用实例 |
| 临床微生物病原学鉴定 | 已知或未知病原体种属鉴定、 病原体全基因组拼接 |
中东呼吸综合征冠状病毒、新型冠状病毒、 伪狂犬病病毒等新型病原体的发掘、 全基因组拼接等 |
| 临床微生物耐药诊断 | 微生物耐药性研究、 微生物与药物相互作用 |
幽门螺旋杆菌克拉霉素耐药基因靶向性检测、 微生物组学数据库的构建等 |
| 临床肿瘤诊治 | 新肿瘤靶标发掘、肿瘤细胞来源、 肿瘤基因低频突变 |
癌症基因图谱重大科研项目创立、 国际癌症基因组计划的进行等 |
| 遗传疾病诊断检测 | 遗传疾病诊断、产前筛查与诊断、 试管胚胎移植等植入性胚胎遗传学诊断 |
智力障碍或残疾畸形儿童产前筛查、 21三体综合征产前筛查等 |
参考文献
[1]Hu T, Chitnis N, Monos D, et al. Next-generation sequencing technologies: An overview[J]. Hum Immunol. 2021, 82(11): 801-811.
[2]Ilyas M. Next-Generation Sequencing in Diagnostic Pathology [J]. Pathobiology. 2017, 84(6): 292-305.
[3]王玉静, 陆梓涔, 陈俊煜, 等.高通量测序技术的发展及其在临床检测中的应用[J].厦门大学学报:自然科学版, 2021.
[4]张丁予, 章婷曦, 王国祥.第二代测序技术的发展及应用[J].环境科学与技术, 2016, 39(9):7.
[5]Zhang H, He L, Cai L. Transcriptome Sequencing: RNA-Seq[J]. Methods Mol Biol. 2018, 1754: 15-27.

相关产品



 苏公网安备32011202001302
苏公网安备32011202001302